AI가 원자 수준의 정밀도로 항체를 처음부터 설계
페이지 정보
본문
(퍼플렉시티가 정리한 기사)
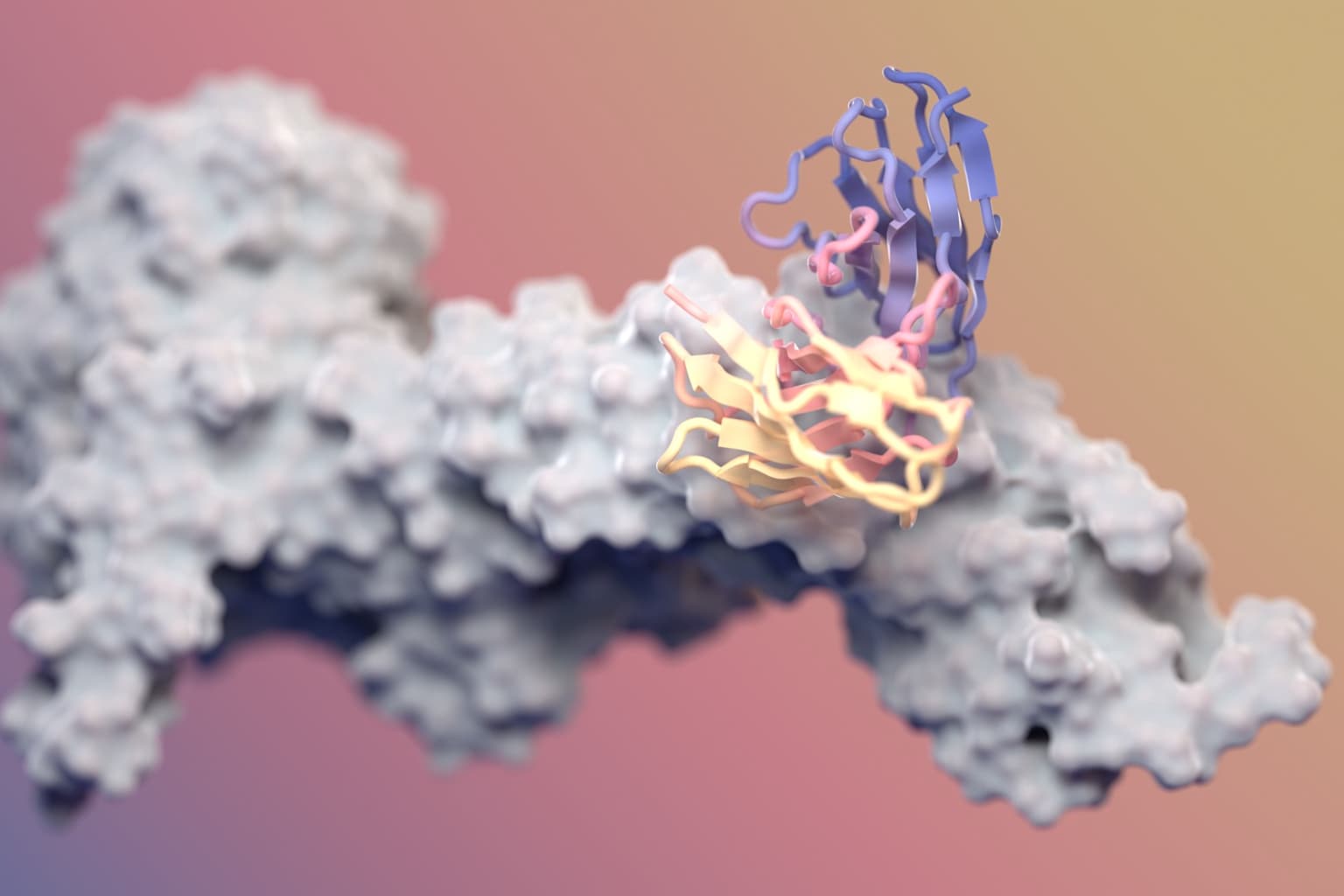
워싱턴 대학교의 노벨상 수상자 데이비드 베이커(David Baker) 연구실에서 인공지능과 생명공학 분야의 혁신적인 돌파구가 나타났습니다. 연구진들이 AI를 사용하여 완전히 기능적인 항체를 처음부터 설계하는 데 성공하며, 전례 없는 원자 수준의 정밀도를 달성했습니다. 오늘 Nature지에 발표된 이 진전은 약물 발견 일정을 수년에서 수주로 극적으로 단축시킬 수 있는 패러다임 전환을 나타냅니다.
이 돌파구는 기존의 자연 템플릿에 의존하지 않고 완전히 새로운 구조를 의미하는 de novo 방식으로 항체를 생성하도록 세밀하게 조정된 정교한 생성형 AI 모델인 RFdiffusion을 중심으로 합니다. 항체의 일부만 수정할 수 있었던 이전 접근법과 달리, 이 AI 시스템은 특정 질병 분자를 표적으로 하는 복잡한 결합 영역인 6개의 상보성 결정 영역(CDR) 모두를 설계할 수 있습니다.
원자 수준의 검증이 혁신적인 정확성을 입증하다
이러한 AI로 설계된 항체의 정밀도는 극저온 전자현미경을 통해 엄격하게 검증되었으며, 구조들이 계산 모델과 탁월한 일치를 보였다. 개별 CDR에 대해 0.3 Å만큼 낮은 평균제곱근편차(RMSD) 값은 설계된 구조와 실제 구조 간의 거의 완벽한 원자 수준 정확도를 보여준다.
Baker 연구실의 박사후연구원 Rob Ragotte는 "컴퓨터로 유용한 항체를 만드는 것은 과학계의 성배였습니다. 이 목표는 이제 불가능한 것에서 일상적인 것으로 변화하고 있습니다"라고 말했다. 이 기술은 클로스트리디움 디피실레 독소 B와 인플루엔자 헤마글루티닌을 포함한 도전적인 표적에 대해 결합 항체를 성공적으로 생성했다.
초기 계산 설계는 적당한 결합 친화도를 보였지만, OrthoRep과 같은 기법을 사용한 후속 최적화를 통해 결합 강도가 한 자리 수 나노몰라 수준—승인된 항체와 비교할 수 있는 임상적으로 관련된 효능—까지 향상되었으며, 동시에 정밀한 에피토프 선택성을 유지했다.
상업적 영향과 산업 변화
이번 혁신은 즉각적인 상업적 파급효과를 갖고 있습니다. 스타트업 자이라 테라퓨틱스(Xaira Therapeutics)가 RFantibody 트레이닝 코드에 대한 독점 라이선스 권리를 확보했습니다. 데이비드 베이커(David Baker)가 공동 창립한 자이라는 10억 달러 이상의 자금과 RFdiffusion 및 RFantibody 모델의 핵심 개발자들을 고용하고 있습니다.
주요 제약회사들은 신약 개발 파이프라인에 AI 역량을 빠르게 통합하고 있습니다. 일라이 릴리(Eli Lilly and Company)는 최근 XtalPi 자회사인 Ailux와 전략적 협력을 발표하고, AI 기반 플랫폼을 활용한 이중특이항체 개발을 추진하고 있습니다. 이 파트너십은 AI가 신약 개발 비용을 최대 40%까지 줄이고, 개발 기간을 50% 단축할 수 있다는 업계 전반의 인식을 반영합니다.
“10년 후 우리는 바로 이런 방식으로 항체를 디자인하게 될 겁니다.”라고 연구 논문의 공동 저자 네이서니얼 베넷(Nathaniel Bennett)은 예측했습니다. 자유롭게 이용할 수 있는 소프트웨어로 항체 설계가 민주화됨에 따라, 글로벌 연구 활동이 가속화되고 특히 소규모 기관과 학계에 큰 도움이 될 것으로 기대됩니다.
이 기술은 감염병, 암 면역치료, 자가면역 질환 등 광범위한 분야에 적용될 수 있으며, 제약업계가 이전까지 ‘공략 불가능’했던 표적에 접근하는 방식을 근본적으로 혁신할 잠재력을 갖고 있습니다. 연구 커뮤니티가 자유롭게 제공되는 RFdiffusion 소프트웨어의 광범위한 도입을 예의주시하는 가운데, 이번 돌파구는 AI가 분석 도구에서 생명을 구하는 치료제의 능동적 창조자로 전환하는 결정적 순간을 의미합니다.